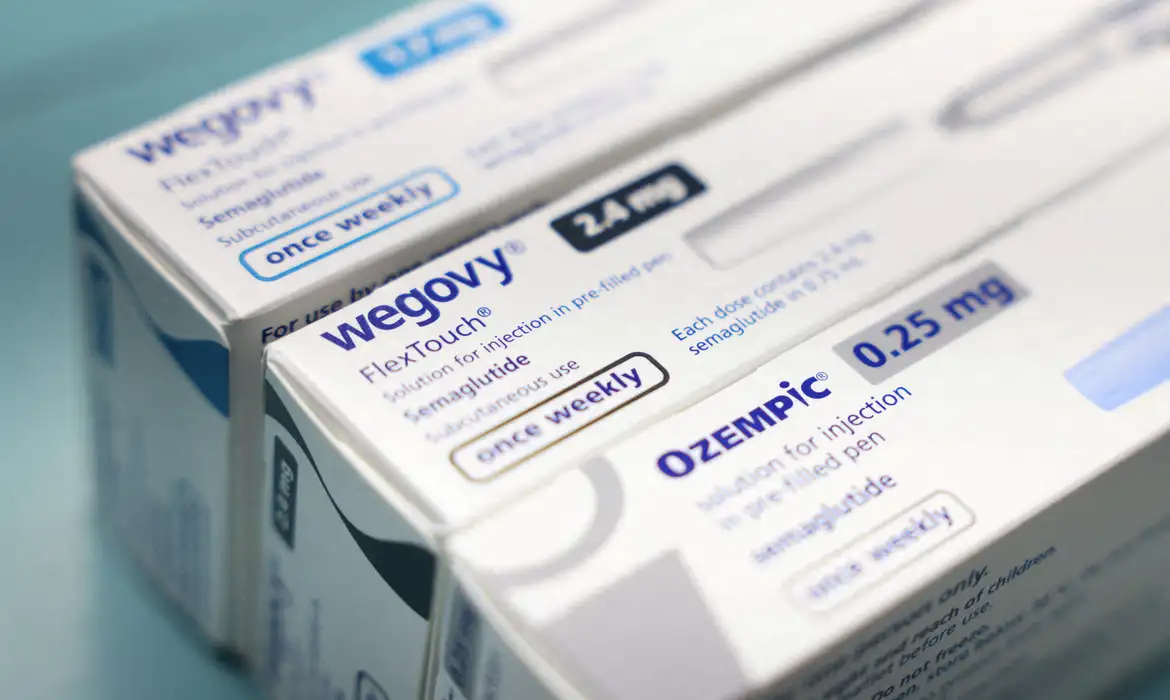
A partir de junho, farmácias e drogarias de todo o Brasil passaram a reter as receitas de medicamentos agonistas GLP-1, popularmente conhecidos como “canetas emagrecedoras”. Essa categoria inclui medicamentos como Ozempic, Mounjaro e Wegovy. A medida, decidida pela diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) em abril, entrou em vigor 60 dias após a decisão.
Com a mudança, a prescrição desses medicamentos agora deve ser feita em duas vias, e a venda só é permitida com a retenção da receita na farmácia, seguindo o mesmo procedimento dos antibióticos. A validade das receitas médicas para essas canetas é de até 90 dias a partir da data de emissão.
Além disso, farmácias e drogarias são obrigadas a registrar a movimentação de compra e venda desses medicamentos no Sistema Nacional de Gerenciamento de Produtos Controlados.
Uso “Off Label” e Preocupações com o Uso Indiscriminado
A Anvisa esclareceu que a nova regra não afeta o direito do médico de prescrever as canetas emagrecedoras para finalidades diferentes das descritas na bula, prática conhecida como uso “off label”. A agência ressaltou que essa é uma decisão de responsabilidade do profissional, com o devido esclarecimento ao paciente.
A retenção do receituário já era uma defesa da Sociedade Brasileira de Endocrinologia e Metabologia, da Sociedade Brasileira de Diabetes e da Associação Brasileira para o Estudo da Obesidade e da Síndrome Metabólica. Essas entidades alertam que o uso indiscriminado desses medicamentos gera preocupações com a saúde pública e dificulta o acesso para pacientes que realmente precisam do tratamento.
Em nota, as entidades destacaram que a venda sem receita médica, apesar de irregular, era frequente. A falta da retenção da receita criava uma lacuna que facilitava o acesso indiscriminado e a automedicação, expondo indivíduos a riscos desnecessários.
Riscos das Versões Manipuladas
Em fevereiro, as mesmas entidades já haviam emitido um alerta sobre os “graves riscos” associados ao uso de medicamentos injetáveis de origem alternativa ou manipulados para tratar obesidade e diabetes. Medicamentos biológicos, como a semaglutida e a tirzepatida, exigem processos de fabricação rigorosos para garantir eficácia, segurança, pureza e estabilidade, especialmente por serem administrados por injeções subcutâneas, que demandam padrões rigorosos de esterilidade e estabilidade térmica.
O uso de versões alternativas ou manipuladas é considerado uma “prática crescente, preocupante e perigosa”, pois carece de bases científicas e regulatórias que garantam sua eficácia, segurança, pureza e estabilidade. Esses produtos não passam pelos testes de bioequivalência necessários, tornando impossível prever seus efeitos no corpo humano e expondo os usuários a sérios riscos à saúde.
Recomendações Importantes
A nota das entidades inclui as seguintes recomendações:
- Para profissionais de saúde: Não prescrever semaglutida ou tirzepatida alternativas ou manipuladas. Devem utilizar apenas medicamentos aprovados por agências reguladoras, com fabricação industrial certificada e vendidos em farmácias.
- Para pacientes: Rejeitar tratamentos que incluam versões alternativas ou manipuladas dessas moléculas (incluindo vendas diretas em sites, aplicativos ou consultórios) e buscar alternativas aprovadas pela Anvisa.
- Para órgãos reguladores e fiscalizadores: Anvisa e conselhos de medicina devem intensificar as ações de fiscalização sobre todas as empresas e pessoas envolvidas nessa prática.
É crucial que pacientes e profissionais de saúde estejam cientes dessas novas regulamentações e dos riscos associados ao uso de medicamentos não aprovados para garantir a segurança e a eficácia dos tratamentos.